La thérapie cellulaire en ophtalmologie

En post-doctorat à l'Université de Rochester (New York, USA), Soumaya Belhadj travaille sur la thérapie de remplacement des photorécepteurs de la rétine et son suivi en optique adaptative. La jeune chercheuse utilise des approches différentes de celles développées en France, à l’Institut de la Vision. Invitée à présenter un séminaire à Paris en décembre 2024, elle revient pour le Guide de la Vue sur ses travaux.
 Soumaya Belhadj
Soumaya Belhadj
Post-doctorante dans le laboratoire de Juliette McGregor, département d’ophtalmologie, Université de Rochester (New York, USA).
Originaire de Lille, Soumaya Belhadj y a mené des études de biologie cellulaire et physiologie. Son stage de fin de licence se déroule à l’Institut Pasteur de Lille, dans l’équipe du Professeur Jean-Charles Lambert qui étudie la maladie d’Alzheimer. Cette première approche des pathologies dégénératives cérébrales incite la jeune femme à s’inscrire en master de Neurosciences à l’Université Pierre et Marie Curie, à Paris. Son stage de fin d’études l’amène à Zurich, où elle profite de sa présence en Suisse pour embrayer sur six mois de stage dans l’industrie pharmaceutique. Après cette expérience au sein du département Auto immunité, transplantation et inflammation de l'Institut de recherche biomédicale Novartis, elle décide de se lancer dans un doctorat. Elle est acceptée dans le laboratoire du Professeur François Paquet-Durand, à l’Université de Tübingen (Allemagne), qui s’intéresse aux pathologies de la rétine. Elle y travaillera, sur des explants rétiniens, au développement de biomarqueurs pour rendre compte de la dégénérescence rétinienne, et ainsi améliorer le diagnostic et le pronostic de ces maladies. L’idée à l’époque est d’aller, à termes, « vers l’injection d’un substrat enzymatique fluorescent, pour visualiser in vivo les zones de dégénérescence des photorécepteurs » détaille Soumaya Belhadj. Une détection qui pourrait se faire grâce à l’optique adaptative, sur laquelle la jeune thésarde a lu un certain nombre de publications. Faute de financement, le projet sera cependant abandonné.
Un goût pour l'imagerie à haute résolution
Son intérêt pour l’imagerie à l’échelle cellulaire va amener Soumaya Belhadj à candidater pour le post-doctorat qu’elle occupe depuis deux ans, au sein de l’équipe de Juliette McGregor, professeure assistante au département d’Ophtalmologie de l'Université de Rochester (New York). Celle-ci s’intéresse notamment à la dégénérescence maculaire liée à l'âge, dans laquelle la perte de l'épithélium pigmentaire rétinien (EPR) et des photorécepteurs (PR) peut mener à la cécité. « Le département d’optique de Rochester est assez prestigieux. Il est connu pour être à l’avant-garde et axé sur l’optique appliqué à la vision. La plupart de mes collègues ne sont pas des biologistes. Juliette est d’ailleurs physicienne, tout comme Elena Gofas et Kate Grieve à l’Institut de la Vision ! » commente la post-doctorante qui se décrit comme une biologiste utilisatrice des techniques optiques développées par ses collègues. Elle les utilise pour observer les transplants qu’elle greffe dans la rétine d’animaux modèles, et évaluer la survie et le comportement des cellules dans le temps. Pour cela elle mobilise l’ensemble des technologies d’imagerie d’usage courant en ophtalmologie (tomographie par cohérence optique (OCT), ophtalmoscope laser à balayage (SLO),…) mais aussi les outils d’optique adaptative conçus par le département d’optique de l’université. « Nous n’utilisons pas d’instruments commercialisés, mais des prototypes, assemblés par les doctorants et ingénieurs en optique qui les fabriquent en commandant chaque lentille, chaque miroir, et les assemblent sur table optique » souligne Soumaya Belhadj.

Instrument à optique adaptative (AO-SLO) pour une imagerie à haute résolution de la rétine © Nabil Rahman
Une collaboration tri-partite
Pour sa recherche, la jeune post-doctorante collabore avec deux autres laboratoires. En amont des expériences se positionne celui de David Gamm, professeur d’ophtalmologie et de sciences visuelles à l’Université de Madison, dans le Wisconsin, et spécialiste des cellules souches. C’est son équipe qui, à partir d’organoïdes dérivés de cellules souches issues d’embryons humains, produit et optimise les populations cellulaires qui vont ensuite être greffées sur des modèles animaux par le pôle chirurgical de l’université de Rochester. Soumaya Belhadj s’occupe ensuite de suivre ces greffons, sur des périodes pouvant aller jusqu’à plus d’un an. Grâce aux différentes techniques à sa disposition, et en particulier l’imagerie par optique adaptative, la post-doctorante revient ainsi, semaine après semaine ou mois après mois, imager les mêmes zones de la rétine chez les animaux transplantés. Pour cela, elle s’oriente dans l’œil grâce aux vaisseaux sanguins, pour retrouver les zones d’intérêt qu’elle a identifié en amont, lors d’un premier examen de fond d’œil. De séance en séance, il lui est donc possible de mettre à jour sa carte de l’œil, pour documenter l’évolution des cellules greffées, du point de vue de leur survie, de leur morphologie…
En bout de chaîne, le troisième partenaire de la collaboration est Teresa Puthussery, professeure associée d’optométrie et de sciences de la vision à l’université de Californie à Berkeley, experte en histologie de la rétine.
C’est son laboratoire qui, à la fin des expériences, récupère les tissus rétiniens pour en faire une analyse in vitro, en microscopie confocale. « L'optique adaptative nous permet de voir les cellules, mais je ne peux pas faire de marquage de type cellulaire puisque nous sommes in vivo. Est-ce qu'il y a des opsines qui sont exprimées ? Est-ce qu'on trouve des marqueurs de connexion synaptique ? C'est elle qui va faire tout le travail en aval sur le tissu fixé, pour déterminer plus en détail la façon dont le transplant à interagit avec les avec les tissus de l’hôte » explique Soumaya Belhadj. Le consortium a reçu pour ce travail un financement du NIH, dans le cadre de son programme Audacious Goals Initiative centré sur la restauration de la vision à travers la régénération de la rétine.
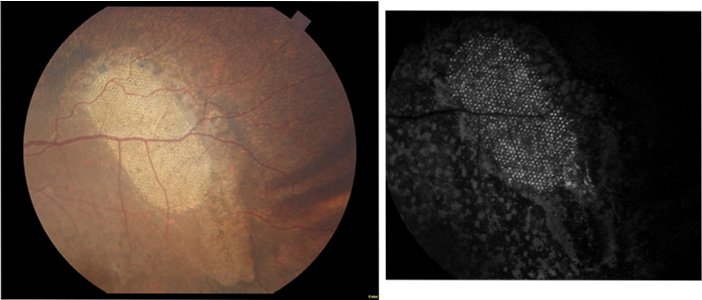
Images du fond de l'œil obtenues 5 semaines après transplantation in vivo. A gauche : le "scaffold" et ses puits en nid d'abeille sont visibles. A droite : en utilisant un filtre spécifique pour tdTomato (gène rapporteur exprimé par les précurseurs) montrant les précurseurs transplantés. © Bill Fischer et Rachel Hollar
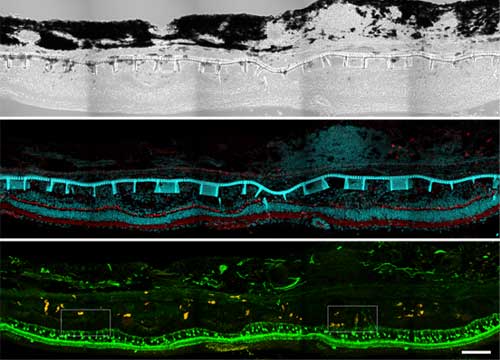
Histologie du tissu rétinien 20 semaines après transplantation obtenue par microscopie confocale à lumière transmise (haut) et à fluorescence (milieu et bas). Le "scaffold" et ses puits sont visibles dans l'espace sous-rétinien dans les 3 images. Image du milieu : vGLUT1 en rouge, marqueur synaptique, marque les couches plexiformes externe et interne. DAPI, en bleu, marque les noyaux cellulaires. Image du bas : tdTomato, en orange, marque les précurseurs transplantés. SCGN, en vert, marque les cellules bipolaires. Ces dernières étendent des prolongements vers les précurseurs transplantés au niveau d'une zone déafferentée, signe prometteur de connectivité entre l'hôte et le greffon. © Laura Patak, Jacqueline Gayet et Teresa Puthussery
Deux approches pour les transplants : la suspension cellulaire…
Parmi les différentes stratégies de thérapie cellulaire, l’une des plus anciennes est l’injection de précurseurs cellulaires en suspension dans l’espace sous-rétinien, dans l’objectif qu’ils recolonisent les espaces laissés vacants par la dégradation rétinienne. Si cette technique a le mérite d’être très peu invasive, elle n’offre que peu de contrôle sur le nombre de cellules qui sont délivrées ou sur leur distribution au niveau de la rétine. Soumaya Belhadj et ses collègues ont donc tenté d’autres approches. L’une d’elle consiste à remplacer le liquide de suspension cellulaire par une solution de fibrinogène. « Plus visqueux, il semble améliorer la répartition
des cellules sous la rétine, mais également leur survie, puisque nous avons pu suivre des transplants à plus d’un an après injection » précise Soumaya Belhadj. Les scientifiques ont ainsi fait l’expérience d’administrer des précurseurs de photorécepteurs (PR) à des modèles animaux ayant des rétines normales ou présentant une ablation sélective de ce type cellulaire. Marqués par fluorescence, puis transplantés par voie sous-rétinienne, ils ont pu être suivis au fil du temps in vivo, de façon non invasive et avec une résolution cellulaire. Cette surveillance a permis de rendre compte de leur survie dans le temps, de leur migration et de la formation de
neurites. L'examen histologique réalisé ensuite par l’équipe de Teresa Puthussery a quant à lui suggéré une migration des PR vers la couche plexique externe et une formation potentielle de synapses dans les zones ablatées de l'œil des animaux receveurs. Autant de signaux encourageants pour l’efficacité de ces approches dans les stratégies de restauration visuelle.


A gauche : image à haute résolution du "scaffold" obtenue in vivo 7 semaines après transplantation par optique adaptative. A droite : au même endroit, image des précurseurs transplantés obtenue par optique adaptative en utilisant un filtre spécifique pour tdTomato (gène rapporteur exprime par les précurseurs). Les flèches indiquent un changement morphologique observé (prolongements à partir des précurseurs transplantés). © Laura Patak, Jacqueline Gayet et Teresa Puthussery.
… et les structures en 3D
Aussi prometteuses que soient les injections de suspensions cellulaires, elles présentent le risque d’une auto-organisation des cellules en rosette qui ne permettrait pas aux précurseurs injectés d’entrer en contact avec l’EPR pour maturer en photorécepteurs fonctionnels. Étant donné la petite taille de la macula (centre de la rétine), et l'importance du contact direct entre l'EPR et les PR pour la survie de ces derniers, une solution attrayante est d’utiliser ce que les chercheurs appellent des « échafaudages ». Ce sont des structures tridimensionnelles construites en polymères approuvés pour un usage chirurgical. Leur forme en nid d’abeille permet la culture de tapis cellulaire de cellules souches qui peuvent être précurseuses d’EPR ou de PR, ou des deux en couches adjacentes. Une fois positionnés dans l’œil, ces échafaudages vont faciliter l’implantation des cellules dans la rétine de l’hôte. « Nous avons deux types d’échafaudage à notre disposition. Tous les deux sont en polyglycérol sébacate, mais ils sont traités différemment, à la chaleur ou à la lumière, ce qui rend l’un deux biodégradable et pas l’autre. Nous sommes actuellement en train de préparer les publications sur ces résultats » détaille Soumaya Belhadj. Faciles à produire, polyvalents et permettant de mieux contrôler le lieu de délivrance des cellules thérapeutiques, ces échafaudages ont le potentiel d’accélérer les efforts de transplantation de cellules rétiniennes pour la thérapie des maladies dégénératives de la rétine. Cependant, de par leur taille, ils nécessitent une incision de la sclère (enveloppe blanche de l'œil) et de la rétine, ce qui en fait donc une chirurgie plus invasive qu’une injection.
S'assurer de la survie, et de la fonction
Pour sa dernière année de post-doctorat dans l’équipe de Juliette McGregor, Soumaya Belhadj veut explorer l’apport de l’imagerie fonctionnelle, via un optorétinogramme, un instrument qui utilise l’optique adaptative pour visualiser la fonction des cônes dans la rétine. « C’est une technique assez récente qui se base sur le fait que quand un cône est stimulé par la lumière, il va changer un peu de taille et de forme. Ce changement de morphologie va se traduire par une modification de la lumière qui est réfléchie par le cône. Et ça on peut le détecter en optique adaptative, cela fait comme un clignotement, qui permet d’établir que les cônes sont fonctionnels » explique la post-doctorante. L’objectif pour elle est pour l’instant de caractériser le comportement d’une rétine saine, par comparaison avec les régions déplétées et greffées, mais également de suivre la récupération fonctionnelle après le décollement de rétine nécessaire à l’injection des transplants. « Lorsque le chirurgien injecte du fibrinogène, que ce soit avec des cellules en suspension ou pour faire de la place pour insérer un échafaudage, cela provoque comme une ampoule, qui se résorbe en une à deux semaines. L’idée est de voir en combien de temps les photorécepteurs récupèrent leur fonction après ce décollement » précise Soumaya Belhadj. Quant à de possibles essais cliniques menés par l’équipe de Juliette McGregor, ils ne sont pour l’instant pas à l’ordre du jour. « Nous cherchons d’abord à voir plus de survie, plus de preuves d’intégration des cellules transplantées. Et nous voulons pouvoir évaluer la récupération de la fonction avant de passer chez l'homme. Même si les patients greffés n’ont plus rien à perdre en termes de vision, cela reste des procédures lourdes, avec traitement immunosuppresseur. Il est bien sur important de démontrer que les transplants sont sûrs et bien tolérés, mais je crois que nous avons encore du chemin à parcourir pour prouver l’efficacité de nos thérapies cellulaires » conclut Soumaya Belhadj.
Propos recueillis par Aline Aurias.
À lire aussi

Dr Masayo Takahashi, pionnière de la thérapie cellulaire régénérative
Une enfance ordinaire, dans la grande métropole d’Osaka au Japon, une scolarité correcte, des parents modestes, personne n’aurait pu prévoir qu’un demi-siècle plus tard Masayo Takahashi serait une des leaders mondiaux de la médecine régénérative appliquée à l’œil.

La dégénérescence maculaire liée à l'âge : DMLA

Les troubles de la vision et les maladies des yeux de A à Z

Phénotypage, génotypage, intelligence artificielle, jumeaux numériques... une nouvelle ère pour la médecine personnalisée
Véritable enjeu de santé publique, les pathologies rétiniennes sont à l’origine de divers handicaps visuels, et de répercussions variables sur la vie sociale et professionnelle des patients concernés.








